
3. Interaksi Antarpartikel

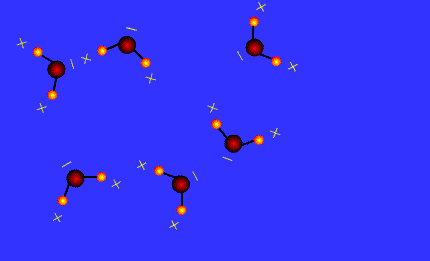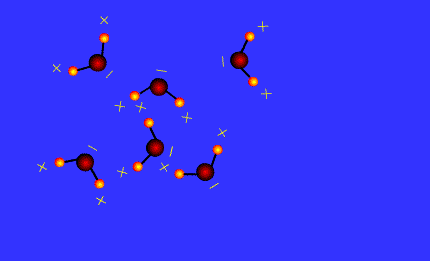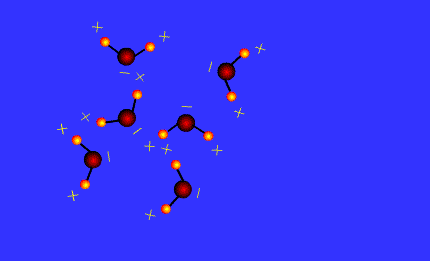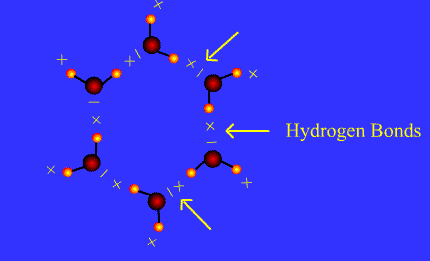
Perhatikan animasi ikatan hidrogen pada sisi kiri dan percakapan nyonya dan tuan chemist pada sisi kanan untuk memudahkan kalian memahami materi pada bab ini.
IKATAN LOGAM
Logam mempunyai beberapa sifat yang unik, antara lain mengkilat, dapat menghantarkan arus listrik dan kalor dengan baik, mudah ditempa, ulet, dan dapat di ulur menjadi kawat. Sifat-sifat logam tersebut tidak dapat dijelaskan dengan menggunakan teori ikatan kovalen maupun ikatan ion. Logam tersusun secara teratur dalam suatu kisi kristal yang terdiri dari ion-ion positif logam di dalam lautan elektron. Lautan elektron tersebut merupakasn elektron-elektron valensi dari masing-masing atom yang saling tumpang tindih. Masing-masing elektron valensi tersebut dapat bergerak bebas mengelilingi inti atom yang ada di dalam kristal tersebut dan tidak hanya terpaku pada salah satu inti atom. Jumlah elektron yang membentuk lautan elektron berasal dari masing-masing atom logam. Gaya tarikan inti atom-atom logam dengan lautan elektron mengakibatkan terjadinya ikatan logam.
Gaya Dipol-Dipol
Gaya dipol-dipol adalah gaya yang terjadi di antara molekul-molekul yang memiliki sebaran muatan tidak homogen, yakni molekul-molekul dipol atau molekul polar. Molekul-molekul polar memiliki dua kutub muatan yang berlawanan. Oleh karena itu, di antara molekul-molekulnya akan terjadi antaraksi yang disebabkan kedua kutub muatan yang dimilikinya.
Pada antaraksi dipol-dipol, ujung-ujung parsial positif suatu molekul mengadakan tarikan dengan ujung-ujung parsial negatif dari molekul lain yang mengakibatkan orientasi molekul-molekul sejajar,